 대한내분비학회 지난 호 웹진 보기
대한내분비학회 지난 호 웹진 보기
Webzine No.44 | 제18권 2호 <통권68호>
2025년 여름호 대한내분비학회 웹진Webzine No.44 | 제18권 2호 <통권68호>
2025년 여름호 대한내분비학회 웹진
김남훈 고려대학교 안암병원 내분비내과
비만은 사실상 대부분의 대사질환을 매개하는 가장 중요한 병리적 표현형이자 위험인자로 잘 알려져 있다. 비만과 더불어 가장 주요한 대사질환인 당뇨병의 관리 및 치료에 관해서는 그동안 상당한 진보가 있었으나, 여전히 평생의 질병부담을 경감할 정도의 획기적 치료는 없는 상태이다. 본 연구실은 비만과 대사질환의 발생 및 진행에 관여하는 메커니즘을 규명하고, 실질적인 치료 전략을 세우고 검증하는 것을 목표로 다양한 임상/전임상/기초 연구를 진행하고 있다. 내분비내과 김신곤 교수님을 필두로 다양한 임상 코호트의 구축, 환자 샘플의 확보, 임상시험의 기획이 이루어지고 있다. 또한, 고려대학교 약리학교실의 비만/대사 연구실 (PI 김동훈 교수님)과의 협업 랩을 구축하여 gut-brain axis와 연관된 다양한 기초 연구가 진행되고 있다.


2형당뇨병은 진단 후 평생에 이르는 질병 부담을 가지는 만성대사질환이다. 따라서 보통 수십 년에 이르는 질환 경과를 가진다. 우리 연구실에서는 2형당뇨병 진단 직후에서 수년 안의 초기 질환 경과가 나머지 수십 년의 관리 및 outcome 발생에 영향을 미친다는 몇 가지 논문을 발표한 바 있다.
이를 바탕으로 2017년부터 새롭게 진단된 2형당뇨병 혹은 당뇨병 전기 환자들의 전향적 코호트 (Anam Diabetes Observational Study, ADIOS)를 구축하였고, 총 350명의 환자가 등록되어 전향적 관찰 과정에 있다. 참가자들은 매년 경구 당부하 검사를 비롯한 체계화된 프로토콜을 적용하여 추적하고 있으며, 동시에 혈청 및 소변 샘플을 획득하였다. 현재까지 주요 연구 결과로는 1) 2형당뇨병 환자의 베타세포기능 변화의 가장 주요한 결정인자는 고혈당 그 자체이며, 2) 섬유모세포성장인자-1 (Fibroblast Growth Factor 1, FGF1)의 혈청 레벨은 베타세포기능과 역의 상관관계를 가지며, 3) 20/30대 젊은 연령 발생 2형당뇨병 환자의 베타세포기능은 진단 초기부터 심각한 결핍 상태에 있다는 것이었다.
현재는 circulating GDF15 (Growth Differentiation Factor 15) 및 FGF4 레벨과 베타세포/인슐린 감수성과의 상관관계, 초기 치료 전략에 따른 베타세포 기능과 인슐린 감수성의 변화 양상에 대한 연구를 진행 중에 있다. 또한 2형당뇨병 유병자들의 대규모 전향적 코호트인 Anam Metabolic Health (AMH) study를 구축하여 심혈관 및 신장 질환에 대한 예측 인자(ketone body, VLDL/IDL cholesterol, NT-proBNP 등)의 유용성을 검증하고 있다.
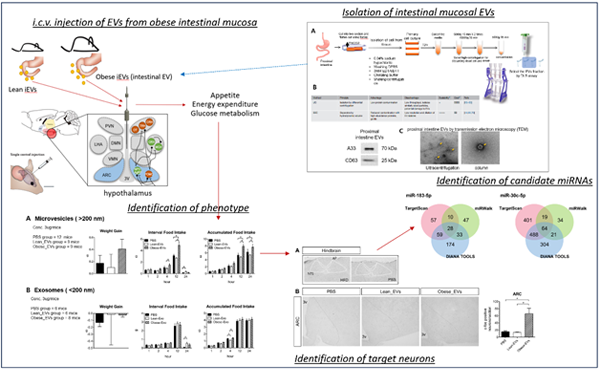
Extracellular vesicle(또는 EV)는 세포가 분비하는 막으로 둘러싸인 입자로, 세포 간의 정보 전달 및 다양한 생리적·병리적 과정에 중요한 역할을 한다. 지방세포 유래 EV (혹은 지방조직 대식세포 유래 EV)가 전신적 인슐린 감수성의 조절에 역할을 한다는 연구가 발표된 이래 대사질환 연구 분야에서 EV의 연구가 활발히 이루어지고 있다. 본 연구실에서는 마우스 모델에서 simplified bariatric surgery 테크닉을 적용하여 십이지장에서 근위부 공장에 이르는 근위부 위장관의 우회가 인슐린 저항성을 감소시킨다는 것을 확인하였고, 이를 바탕으로 근위부 위장관 점막 유래 EV (imEV)가 식욕 및 당대사에 미치는 영향을 확인하는 연구를 진행하였다. 비만 마우스 모델에서 분리한 imEV를 뇌실내 투여하였을 때, 특정 분획 (>200nm)의 EV가 식욕 및 식이섭취를 유의하게 감소시키며, 이는 시상하부 궁상핵의 전기적 신호 활성화를 유도하였다. imEV에 대한 small RNA sequencing을 통해 식욕 조절과 관련한 후보 miRNA를 특정하여 후속 연구를 진행 중에 있다. 궁극적으로 식욕 조절에 대한 gut-brain axis에서 위장관 유래 EV의 역할이 존재함을 증명하고자 한다[그림 1].
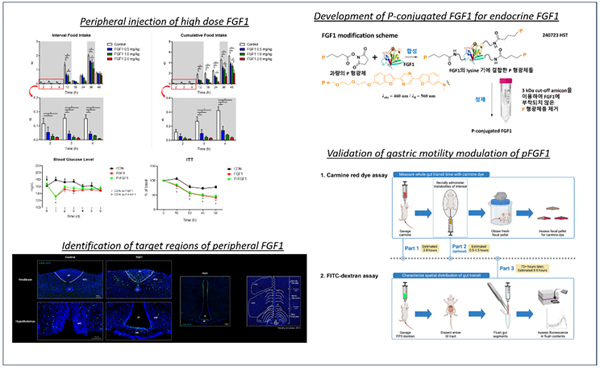
FGF1은 FGF family에 속하는 단백질로, 다양한 세포의 증식, 분화, 생존, 조직 재생 및 대사 조절에 관여하는 다기능성 성장인자이다. FGF1은 acidic FGF라고도 불리며, FGFR (fibroblast growth factor receptor)과 결합하여 downstream signaling pathway를 활성화하는데, 대표적으로 MAPK/ERK, PI3K-Akt, PLCγ 경로 등이 있다. 특히 최근 대사 연구에서는 FGF1의 중추신경계 내 역할이 주목받고 있다. 뇌의 시상하부 특히 궁상핵 등 대사 조절 영역에 FGF1을 주입하면, 혈당 강하 효과가 장기간 지속되며, 이 효과는 인슐린 비의존적으로 작용한다는 점에서 제2형 당뇨병의 새로운 치료 타깃으로 제안되고 있다. 본 연구실에서는 FGF1의 실질적인 항당뇨, 항비만 치료제로서의 역할을 검증하기 위해 말초 전달을 통한 표현형의 변화를 검증하였고, 용량의존적으로 체중과 인슐린 감수성을 개선시키는 것을 확인하였다. 뇌내 hindbrain의 타깃 부위를 특정하였고, 이는 incretin based drug 과 유사한 영역의 활성화였다. 후속 연구로 1) FGF1의 lysine기를 hydrophobic 형광물질로 대체하여 endocrine effect를 활성화시키는 P-conjugated FGF1의 개발, 2) FGF1의 gastric motility에 미치는 영향을 검증, 3) 궁극적으로 항비만 치료제로서 FGF1의 역할 검증을 목표로 하고 있다[그림 2].
본 연구실은 역사가 길지 않고, 그렇기 때문에 작지만 의미 있는 연구의 걸음마를 딛고 있다. 연구실의 모든 구성원들은 임상과 기초가 자유롭고 유기적으로 연결되는 연구 환경을 만들어, 지금 이 순간에도 고군분투하는 젊은 연구자들에게 하나의 본보기가 되었으면 하는 바람을 가지고 있다.