인하대학교 의과대학
대사질환네트워크연구실
김경진 (인하의대 대사질환네트워크 연구실)
1. 연구실 개요
본 연구실은 인하대학교 의과대학 60주년기념관에 위치하고 있으며, 2019년 9월에 설립된 신생 연구실이다. 현재 연구책임자인 김경진 교수와 1명의 선임연구원, 4명의 석사, 박사과정학생으로 구성되어 있는 작은 연구실이다.
기본 연구실 공간, 세포배양실과 학생공간으로 구성된 작은 실험실이지만, 기본적인 분자생물학, 생화학 실험에 필요한 장비와 선도연구센터 및 의과학연구소로부터 구축되어 있는 공동실험 장비를 활용할 수 있어 연구의 진행에 필수적인 대부분의 장비를 갖추고 있다. 규모가 크고 많은 연구원으로 구성된 실험실과 비교하면 매우 소규모인 연구실이지만, 대사질환에 대한 이해와 치료를 위한 기반 구축에 기여하겠다는 큰 포부를 가지고 연구를 진행하고 있다. 각 구성원별로 독립된 연구 프로젝트를 가지고 인하대학교 내 다른 연구팀, 국내 타대학/연구소 및 기업체와의 공동연구 뿐만 아니라, 미국 콜롬비아 대학 및 이탈리아 그룹과 국제 공동 연구 수행을 통해 작지만 발전하는 연구팀이 되고자 노력하고 있다.
2. 주요 연구 내용
(1) 지방간 및 지방간염을 조절하는 표적유전자 발굴 및 역할 규명
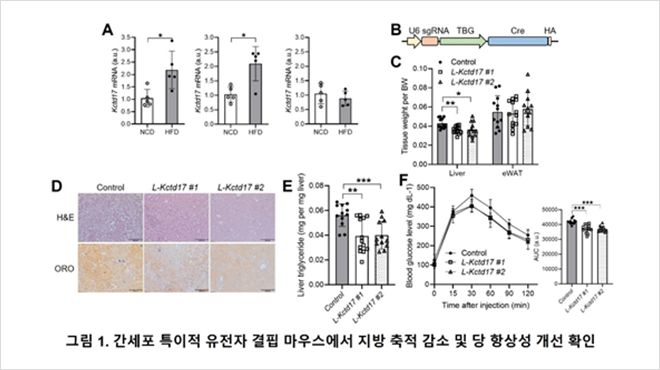
고령화와 비만율의 증가는 인슐린 저항성, 2형당뇨병 및 비알코올성 지방간 (nonalcoholic fatty liver disease, NAFLD)과 같은 대사 질환 증가의 주요한 원인으로 알려져 있다. 본 연구실에서 주로 연구하고 있는 비알코올성 지방간/비알코올성 지방간염 (nonalcoholic steatohepatitis, NASH)은 가장 흔한 간질환으로 타겟 발굴 및 치료 방법 개발에 어려움을 겪고 있어 아직까지 승인된 치료제가 없는 질환이다. 따라서 본 연구실에서는 liquid chromatography-tandem mass spectrometry (LC-MS/MS) 또는 RNA sequencing을 통해 NAFLD/NASH 모델에서 표적 유전자/단백질을 발굴하고 이에 대한 기능을 연구하는 연구를 수행하고 있다. CRISPR/Cas9 시스템을 이용한 조직/세포 특이적 유전자 결핍 동물 및 세포 모델, 간 특이적 유전자 과발현 시스템을 구축하여 발굴된 표적인자의 기능을 검증하고, 표적인자의 발현을 조절하는 상위 신호가 무엇인지 이해하는 것이 주요 연구 목표이다. 최근 연구 결과에서는 간세포 특이적 표적인자 결핍 마우스 모델의 구축을 통해 NAFDL/NASH를 제어할 수 있는 새로운 인자를 발굴하고 그 기전을 밝힘으로써 (그림 1), 궁극적으로 상위 단계에서 유전자 및 단백질 조절 기전에 대한 이해를 통해 지방간/지방간염을 조절할 수 있는 새로운 치료전략을 발굴할 수 있을 것으로 기대하고 있다.
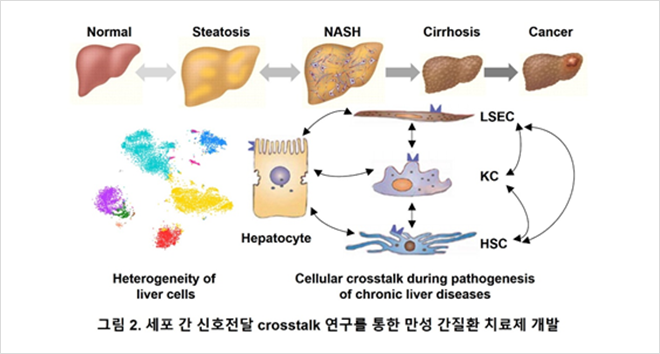
(2) 세포 간 신호전달 crosstalk 연구를 통한 만성 간질환 치료제 개발
간은 간세포 (hepatocyte), liver sinusoidal endothelial cell (LSEC), Kupffer cell (KC), hepatic stellate cell (HSC), cholangiocyte 등 다양한 세포로 구성되어 있다. 특히 간세포는 간 전체의 약 60% 이상을 차지하고 있으며, 초기 간질환에서 지방 축적이 나타나는 주요한 세포이지만, 만성 간질환의 진행에서 다른 세포에 미치는 영향 및 다른 세포에 의한 기능 변화에 대해서는 아직까지 잘 알려져 있지 않다. 본 연구실에서는 초기 및 만성 간질환 모델에서 전사체 분석을 포함한 멀티오믹스 (multiomics)를 활용하여, 단백질 발현 및 활성 변화를 분석하고, 간세포와 주변 세포 교신을 조절하는 새로운 분비 단백질을 규명, 그 기능을 연구하고 있다 (그림 2 참고). 간세포 특이적 유전자 결핍 마우스 모델, organoid, spheroid 및 미니 간 (mini liver) 모델 개발 및 활용을 통해, 만성 간질환을 유도하는 조절 인자를 발굴하여 초기에 질환을 예측하고 예방 및 치료를 위한 약물 개발에 기여할 수 있을 것으로 기대하고 있다. 현재 몇 가지 단백질을 위주로 다양한 세포 간 crosstalk에 미치는 영향을 다각적으로 분석하고 있어 흥미로운 연구 결과를 기대하고 있다.
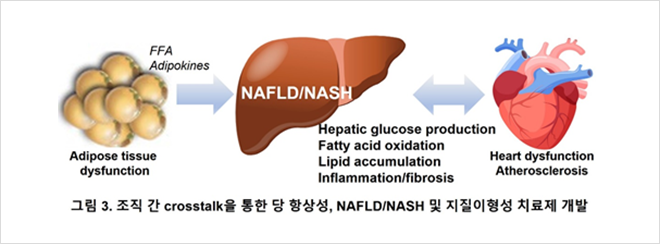
(3) 조직 간 crosstalk을 통한 당 항상성, NAFLD/NASH 및 지질이형성 치료제 개발
본 연구실의 또다른 연구 주제 중 하나는 조직 간 crosstalk을 통해 대사질환을 조절하는 새로운 표적인자를 발굴하고 그 기능을 규명하는 연구이다. 지방조직은 “bona fide” 내분비 기관으로 시스테믹한 대사 항상성을 조절하는 중요한 기능을 담당하고 있다. 본 연구실에서는 지방세포로부터 유래되는 대사물질이 간과 같은 주변조직과의 communication을 통해 시스테믹한 당 항상성 및 NAFLD/NASH에 미치는 영향에 대한 연구를 수행하고 있다. 특히, 지방세포 분화 및 분해과정을 조절하는 표적 유전자를 규명하고 조직 특이적 유전자 결핍 동물 및 세포 모델을 활용하여 기능을 검증하는 연구와 표적 유전자에 의한 비만 및 2형당뇨병 조절 유도 기전 규명을 통해 새로운 대사질환 치료전략 개발에 기여할 것으로 기대하고 있다.
또한 지질이형성 및 동맥경화를 유도하는 표적유전자 발굴 및 기능 검증을 통해서, 심혈관 질환 완화를 위한 치료제 개발 연구를 진행하고 있다 (그림 3 참고). 특히, 간세포에서 리포프로테인 (lipoprotein)의 작용 기전에 관심을 가지고 이를 조절할 수 있는 상위 신호전달체계를 구축하는 연구를 통해 치료제 개발을 위한 새로운 전략을 제시할 수 있을 것으로 생각된다.
3. 맺음말

앞에서 소개 드린 연구 이외에도 본 연구실은 대사질환 연구 및 치료제 개발을 위한 모델 개발을 통해 약물 표적 스크리닝 시스템 구축 및 기업체와의 협력을 통해 지방간염 완화를 위한 표적 발굴 프로젝트를 수행하고 있다. 작은 실험실이지만, 의미 있는 연구 성과를 통해 실제 환자들에게 도움이 될 수 있는 치료제를 개발하는 것을 목표로 앞으로도 꾸준한 연구를 진행하고자 한다. 본 연구실은 현재 선임연구원인 오아름 박사, 정예린, 정영훈, 기현준 박사과정 학생 및 김영운 석사과정 학생들로 (그림 4) 구성되어 각자의 연구주제를 가지고 대사질환 제어기전에 대한 다양한 연구를 진행하고 있다.
연구실 홈페이지: https://sites.google.com/view/mdn-lab
4. 대표논문